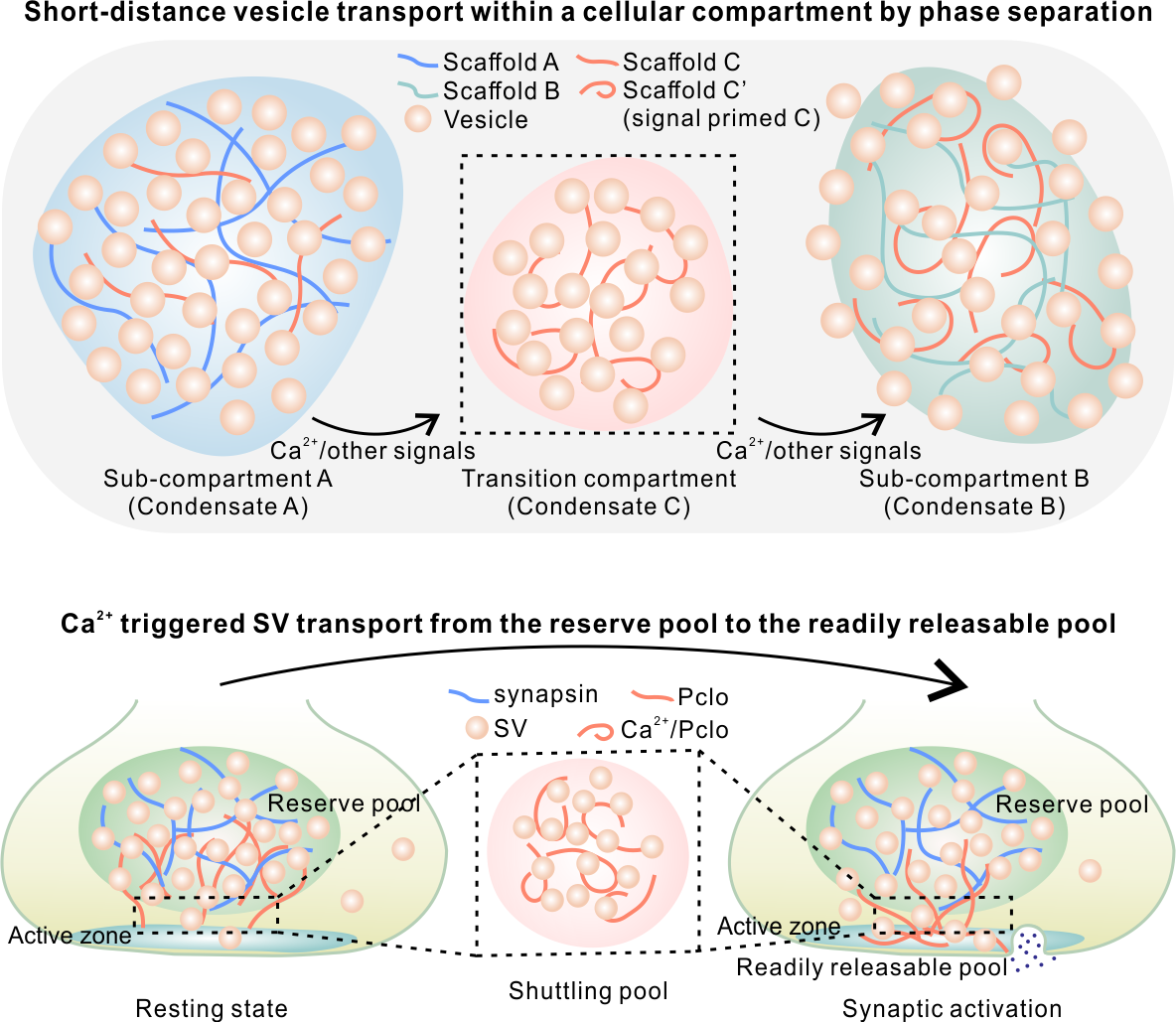
香港科技大学(科大)的研究团队揭示囊泡在细胞内局部区域进行短距离运输的机制,为这个生物学家尚未充分认识的领域提供了新方向。
囊泡是一个小的细胞容器,可以执行多种生物功能,包括转运蛋白质、脂质、以及生物体生存所需的其他物质,并回收废料。 除了使用马达蛋白进行长距离运输外,细胞还有在特定区域进行短距离囊泡运输的需求。 然而,这种短距运输的确切机制仍待科学家进行研究。
为了应对这项挑战,一支由科大生命科学部博士研究生裘骅先生及研究资助局博士后研究员吴先登博士所带领的研究团队,在科大前生命科学部讲座教授张明杰和科大生命科学部教授邬振国的指导 下,聚焦于突触囊泡(SVs)的研究,成功揭开了短距离运输的神秘面纱。 他们发现,这些与囊泡相关的特定蛋白质的相分离,能够使囊泡在细胞的不同区域之间以可控的方式移动。
具体而言,一种名为Piccolo的巨型条状蛋白质,可以响应钙讯号,从储备池(reserve pool)提取突触囊泡,并将它们运送到活跃区域(Active zone)。
他们还发现,另一种名为TFG的蛋白质也透过使用类似的相分离过程,协助囊泡从内质网(ER)运送到内质网-高尔基体中间体。
有见及此,研究结果表明,相分离或是细胞调控囊泡以特定方向短距离运输的通用方式。
在细胞中,囊泡需要沿着特定方向移动以满足各种生理需求,细胞不同区域之间的长距离运输主要依赖细胞骨架和马达蛋白,而囊泡也需要在细胞中一些比较局部的区域内进行 短距离运输。 例如,在高尔基体中,囊泡需要在间隔几百纳米的腔室间快速移动,以进行蛋白质的加工与分选。 同样,在神经细胞末梢,突触囊泡则需要在数百纳米范围内从储备区转运到释放位点,以控制神经递质精确释放。
与长距离囊泡运输相比,现时人类除了知道这个过程不涉及马达蛋白外,对细胞如何实现局部的囊泡定向运输机制所知甚少。 因此,此项研究引证了细胞内帮助囊泡在特定方向上进行局部短距离运输的过程,成果至关重要。
吴博士表示:「我们的研究证明,在无需马达蛋白的参与下,囊泡的短距离定向运输可以透过相分离来实现,能在广泛的细胞生物学领域场景中应用。因此,如何将新的 囊泡运输机制拓展至其他已知的细胞过程中,将会成为重要的未来研究方向。」
是次研究题为「相分离介导短距离囊泡运输」,已于科学期刊《细胞》上刊载。