由香港科技大學(科大)生命科學部和化學及生物工程學系劉凱教授領導的研究團隊,成功開發了一種顱內橄欖頂蓋前核(OPN)前視神經束損傷模型(pre-OPN OTI),並揭示了重塑受損中樞神經系統功能性環路的關鍵機制,為神經創傷以及神經退行性疾病的精準治療提供了嶄新方向。
成年哺乳動物的中樞神經系統(CNS)一旦損傷,其自我修復能力較低,主要原因在於損傷後神經軸突無法再生,亦無法與目標神經元重建功能性連接。目前的研究多聚焦在增強軸突再生能力,但僅有少數模型能在完全性損傷後實現功能性連接,而且重建功能性連接機制仍不明確。為此,劉凱教授的團隊展開相關研究,成功開發了顱內橄欖頂蓋前核前視神經束損傷模型,該研究結果於2025年3月在《Nature Communications》上發表,題為「Functional optic tract rewiring via subtype- and target-specific axonal regeneration and presynaptic activity enhancement」。
該模型通過顯微手術在小鼠外側膝狀體(LGN)與OPN間施加機械壓力,精確地使小鼠視網膜神經節細胞(RGCs)軸突受到損傷。相較於傳統模型,該模型有幾個顯著優勢──無需移除皮層組織,手術時間縮短;損傷位點距離靶核團OPN接近,便於研究靶向軸突再生;利用瞳孔光反射(PLR)作為功能恢復指標,實現定量評估;RGCs存活率高,可作長期觀察。研究透過完全喪失PLR以證實損傷的完整性(因PLR由內在光敏視網膜神經節細胞ipRGCs經OPN環路介導),並通過瞳孔收縮定量監測功能恢復進程。
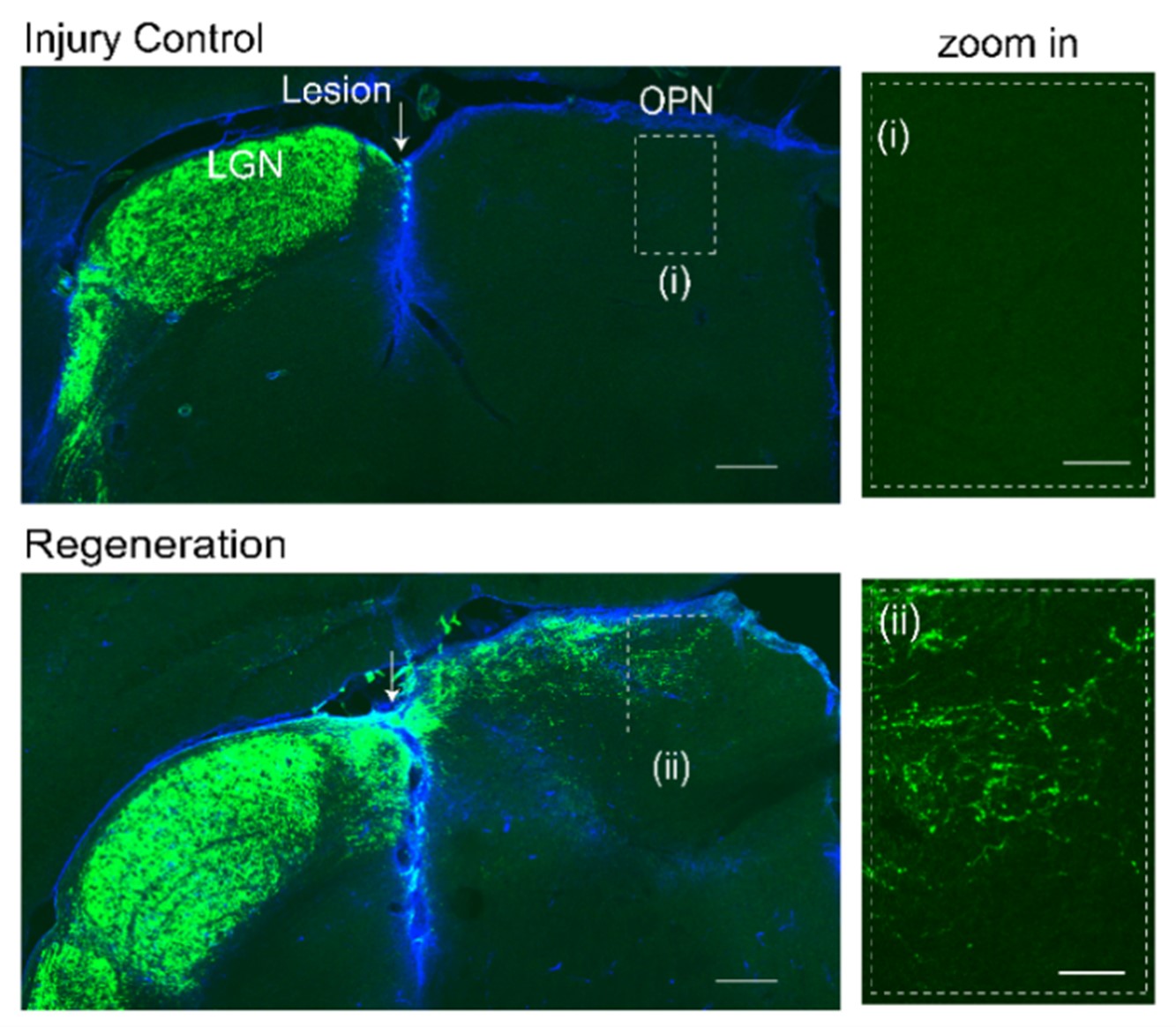
研究團隊發現,通過敲除RGCs的Pten/Socs3基因並同時表達CNTF,可顯著促進軸突再生至OPN並重建功能性突觸(圖二)。功能性環路重建的證據包括:超解析度顯微鏡顯示突觸前與突觸後的突觸標記物共定位、電鏡觀察到再生軸突與OPN神經元建立完整的突觸結構、跨突觸病毒示蹤與電生理記錄驗證突觸傳遞功能恢復,以及PLR的部分恢復顯示重建功能性連接。值得一提的是,ipRGCs被確認為功能恢復的核心視網膜神經節細胞類型,其再生軸突能精準重連原始靶點。
為提升再生效率和功能恢復,團隊提出「軸突再生 + 突觸功能增強」雙重干預策略:結合敲低脂代謝基因Lipin1、敲除Pten/Socs3及表達CNTF,使軸突再生速度加快,PLR恢復時間從6個月縮短至3個月 ; 透過表達黑視蛋白(melanopsin)增強RGCs光敏性,或增強突觸前鈣離子通道活性,可進一步提升突觸信號傳遞效率,顯著改善功能恢復效果。因此,pre-OPN OTI模型為CNS修復研究提供重要的工具,不僅闡明了特定神經元類型(ipRGCs)在功能環路重建中的關鍵作用,並驗證了雙重干預策略的應用潛力。這成果不僅深化了對CNS再生機制的理解,也為神經創傷以及神經退行性疾病的精準治療提供了新方向。
研究由科大劉凱教授的研究團隊領導,聯同電子及計算機工程學系和化學及生物工程學系王怡雯教授的團隊,以及多間大學的研究團隊合作完成,包括香港中文大學姜裡文教授、段麗婷教授,香港城市大學容永豪教授,中國科學技術大學馬玉乾博士。科大生命科學部張欣博士、研究助理教授楊超、博士生張承樂為文章共同第一作者,劉教授為通訊作者。相關工作得到香港研究資助局、香港創新科技署和國家自然科學基金等項目支持。