科大研究团队共同发现内质网融合蛋白新功能 为了解遗传性痉挛性下身麻痹病理提供新见解
香港科技大学(科大)和中国科学院(中科院)生物物理研究所的研究人员,近日发现一种名为atlastin(ATL)的酶,原来具有运送细胞内蛋白质的功能。这项全新发现有助了解遗传性痉挛性下身麻痹(HSP)﹕一种因神经缺陷而引致下肢痉挛的罕见遗传性疾病背后的病理。
科学界已知ATL与导致HSP有关,但出现突变的ATL如何影响正常生理机能运作仍是一个谜。最近,由科大理学院生命科学部助理教授郭玉松领导的团队,发现了缺乏ATL的细胞,会严重推迟一些重要蛋白自细胞当中被移送至细胞表面的过程,从而导致我们的生理机能失灵。团队亦揭示了一个有趣现象,便是一种经过改造的ATL,能纠正以上的情况,为寻找此遗传性疾病的治疗方法提供了新见解。上述成果由中科院生物物理研究所胡俊杰教授的团队共同发现。
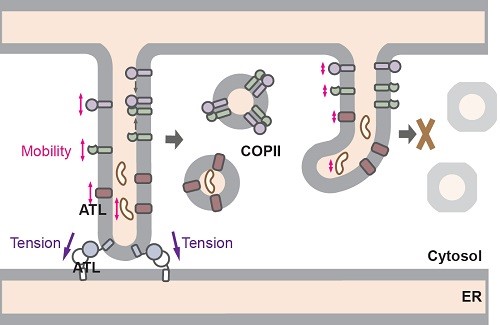
胰岛素、人类抗体或依附在细胞表面负责接收讯号的蛋白,一旦在细胞中形成,便需透过分泌运输途径被输送至细胞表面,以执行各项身体所需的功能。这些蛋白首先被装载至COPII囊泡这种运输工具之中,然后经第一站「内质网(ER)」出发,最终被传送至细胞表面。
内质网的管状结构由dynamin超家族蛋白atlastin(ATL)接驳而成。郭教授及其合作伙伴利用崭新的CRISPR/Cas9技术消除ATL后,发现缺少了ATL的细胞,其内质网管道不但无法接驳得上,COPII的形成亦告减少,影响其装载蛋白的效率。事实上,很多内质网的出口位置亦失去招募COPII载体的能力,严重减慢蛋白的运送速度。研究亦进一步发现,蛋白质的流动性以及COPII的形成,可透过一种经过异变、具膜栓连而非融合功能的ATL来恢复。有关研究成果近日于科学期刊《美国国家科学院院刊》中发表(https://www.pnas.org/content/early/2019/06/24/1908409116)。
郭教授指出,有关研究为ATL出错可如何导致遗传性痉挛性下身麻痹症提供了新见解。他表示:「很明显, ATL介导的膜栓连在维持蛋白于内质网结构内的流动性方面保有关键作用,虽然我们并无相关的医学知识制订治疗策略,但我期望是次发现可为这罕见疾病的治疗方法提供线索。」
郭教授是研究细胞内部运输方向的专家。有关研究的资金由研资局和国家自然科学基金委员会提供。
有关香港科技大学
香港科技大学(www.ust.hk)是国际知名的研究型大学,其科学、工程、商业管理及人文社会科学领域,均臻达世界一流水平。科大校园国际化,提供全人教育及跨学科研究,培育具国际视野、创业精神及创新思维的优秀人才。科大的研究于香港的大学教育资助委员会「2014研究评审工作」获得最多「世界领先」评级,亦于最新的《泰晤士高等教育全球年轻大学排名榜2019》中排行第一,而科大的毕业生在2017年度的全球大学就业能力调查排名第12位,位列大中华院校之首。
传媒查询:
林淑媛
电话﹕2358 6313
电邮﹕anitalam@ust.hk
黄津琪
电话﹕3469 2512
电邮﹕jamiewong@ust.hk