香港科技大学(科大)研究人员发明了一种名为「CarGAP」的突破性微观通道调控工具,可利用维生素B₁₂和绿光精确控制间隙连接,使细胞之间得以直接而可控地进行通讯。通过精确、按需要地关开细胞间的桥梁,这项新技术为调控细胞间关键分子和电讯号的流动提供了前所未有的时空精度。该工具已在哺乳类动物细胞和活体果蝇中得到验证,为研究发育、免疫及神经活动提供了有效的新途径,并对理解疾病机制和推进再生医学研究具有深远潜力。
间隙连接对维持生命基本功能至关重要。这些通道负责细胞间离子、第二信使和小分子的直接传递,从而协调包括心跳与大脑功能在内的多种细胞活动。当间隙连接功能失调时,可能引发心血管疾病、发育异常,甚至癌症。然而,研究其精确功能一直颇具挑战。传统的基因敲除方法具有不可逆转且不够精确的限制,而化学抑制剂则往往缺乏特异性,并可能产生毒性。因此,开发一种能够如开关般进行精细、低副作用地调控间隙连接技术,已成为细胞生物学和神经生物学领域长期的关键需求。
研究的核心挑战在于建立一种既可逆转且具生物兼容性、又不干扰细胞自然过程的间隙连接调控策略。现有的光遗传学工具多依赖具有潜在光毒性的蓝光,而化学方法则普遍缺乏空间精确度。基于上述限制,研究团队因此致力开发一套可基因编码、能响应无害刺激、并可广泛应用于从人类细胞到复杂模式生物(如果蝇)的通用调控系统。
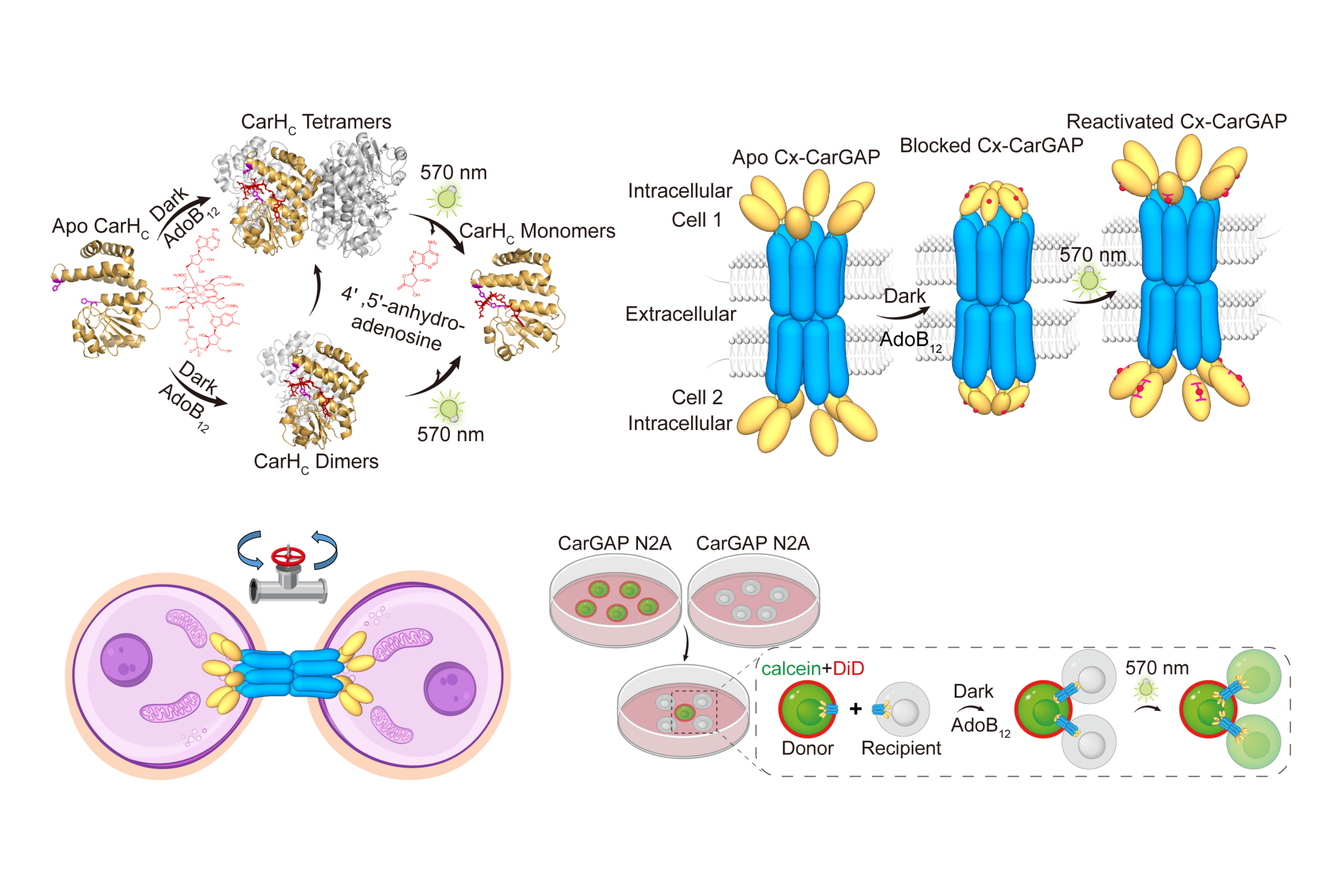
由科大化学及生物工程学系教授孙飞教授、嘉里理学教授兼生命科学部讲座教授解亭教授、生命科学部前研究助理教授屠仁军教授(现为南京东南大学教授),以及北京大学化学与分子工程学院邹鹏教授合作领导的团队,通过将间隙连接蛋白(脊椎动物的连接蛋白connexins和无脊椎动物的innexins )与一种来自细菌CarHC蛋白的光敏维生素B₁₂结合域融合,成功开发出CarGAP系统。在黑暗条件下,添加维生素B₁₂( AdoB₁₂ )会诱导CarHC结构域发生寡聚,从而物理性堵塞通道;而施加柔和的绿光( 570 nm )则可促使这些蛋白阻塞物解聚,重新开放通道。这一精巧设计使研究人员能通过简单的维生素实现通道关闭,再通过光照实现通道重新开启。
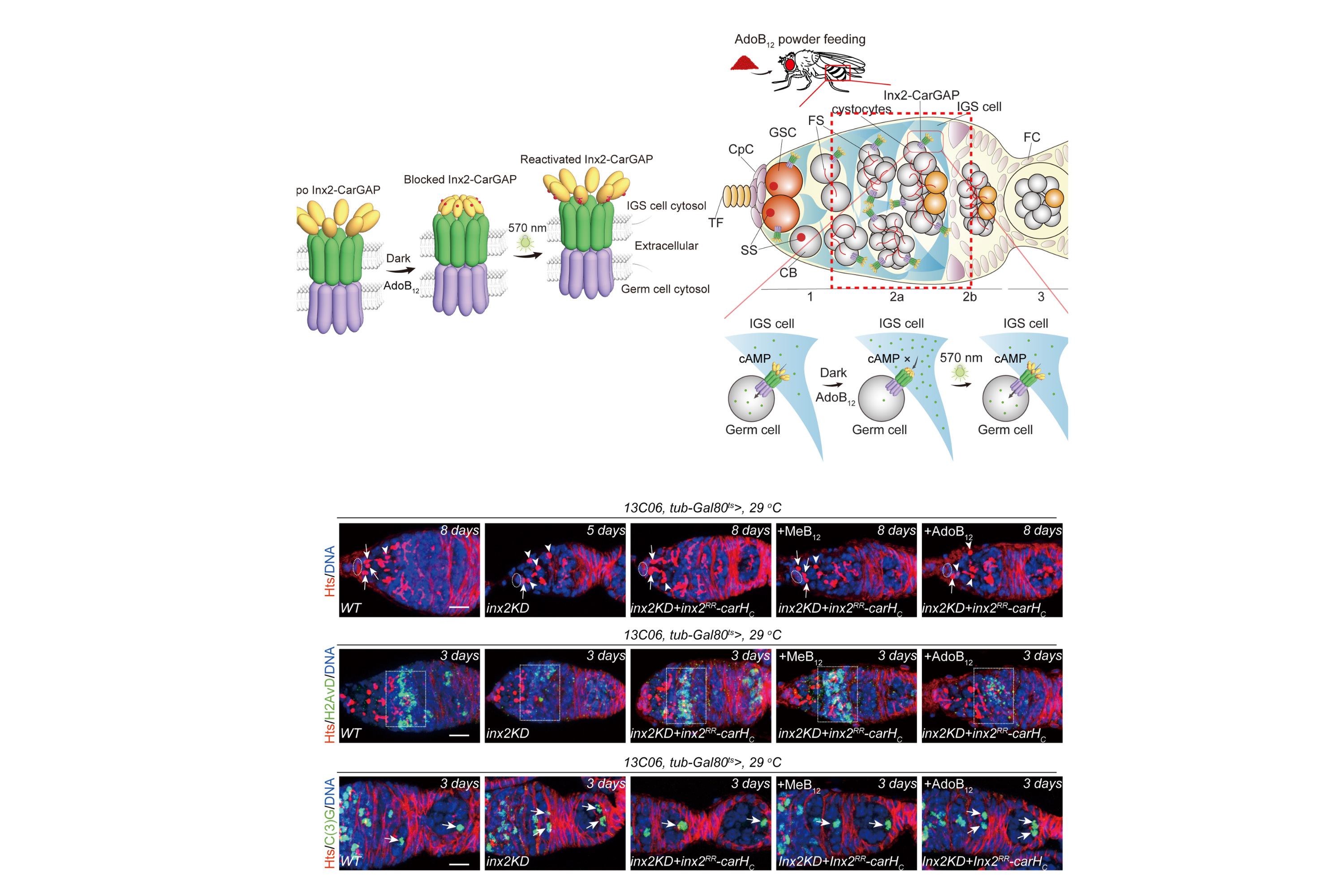
研究团队在多个层面上验证了CarGAP的功能:他们成功调控了荧光染料及免疫信号分子2'3'-cGAMP在哺乳类动物细胞间的传递,并利用远红电压传感器NAVI-Cy5,光学记录了光照后细胞间电耦合的恢复。最令人瞩目的是,团队将CarGAP引入活体果蝇卵巢,成功阻断了干细胞与支持性微环境细胞之间关键信号分子cAMP的流动,并在光照后恢复其流动,从而直接影响了干细胞行为及卵子发育过程。
孙飞教授表示:「CarGAP为我们提供了一种能够远程操控细胞最基础通讯模式的工具。通过结合维生素B₁₂的生物兼容性与光调控的精准性,我们现在可以实时探究细胞如何协调行为——无论是在胚胎、大脑还是肿瘤中。这项工具为理解细胞的动态语言打开了一扇新的窗口。」
这项研究成果已於《美国国家科学院院刊》上发表,论文题为「维生素B₁₂与光协同调控的间隙连接」。研究的共同第一作者包括孙教授的博士生崔舵、黄鑫彧,以及北京大学博士后研究员刘书彰博士。