研究揭示DNA解旋機制 為癌症治療帶來新曙光
香港科技大學(科大)聯同香港大學(港大)與法國居禮研究所共同發現了人體MCM2至MCM7蛋白複合體(Minichromosome Maintenance 2-7,微小染色體維持蛋白2-7)調控DNA 複製起始(Replication Initiation)的新機制。 此發現可被應用於研發新型、高效及更具針對性的抗癌藥物。這項研究成果現已刊登在國際頂尖科學期刊《細胞》雜誌上(按此瀏覽期刊文章)。
我們的生命由單個受精卵細胞形成時開始。在母體子宮內,受精卵通過細胞分裂而發育成多細胞個體。在每次分裂中,編碼遺傳信息的基因組DNA都會被準確複製。每個細胞攜帶的DNA總長度約為兩米,其通過摺疊、整合成為23對染色體。在人的一生中(約70年),人體將合成接近一光年長度的DNA(10^16米)。在複製的過程中,首先須利用解旋酶將雙鏈DNA分解成兩條單鏈DNA,其後DNA聚合酶以此為模板,合成兩條新的互補配對的雙螺旋DNA。若調控過程中出現一絲紊亂,都可能導致嚴重後果,例如腫瘤或遺傳疾病等。
「破解DNA複製的機制是認識生命奧秘的關鍵。」領導這項研究的港大生物科學學院助理教授翟元樑博士說。「而解析複製機器蛋白質結構是了解其分子功能最核心的步驟,因為只有親眼看到,才能相信。」
自1953年詹姆斯‧華生和弗朗西斯‧克里克解析DNA雙螺旋結構以來,DNA雙鏈最初是如何被解旋並打開,一直是個未解之謎。1983年,本研究的合作夥伴、康奈爾大學的戴楊碧瓘教授在釀酒酵母中發現了真核生物的DNA解旋酶基因—— MCM 。 隨後的研究發現,六個MCM基因編碼、由MCM2至MCM7蛋白形成的一個六亞基環狀複合體,構成DNA解旋機器的活性中心。在細胞體內,DNA複製的起始須要由MCM2-7首先組裝到染色體上成千上萬個複製原點,並形成環繞雙螺旋DNA的雙六聚體(double hexamer, DH)。其後,一部分的MCM 2-7 DH被激活成為高效的DNA複製解旋酶。一直以來,研究人員認為MCM2-7 DH具有直接解旋和打開雙鏈DNA的能力,但其作用機制尚不清楚。
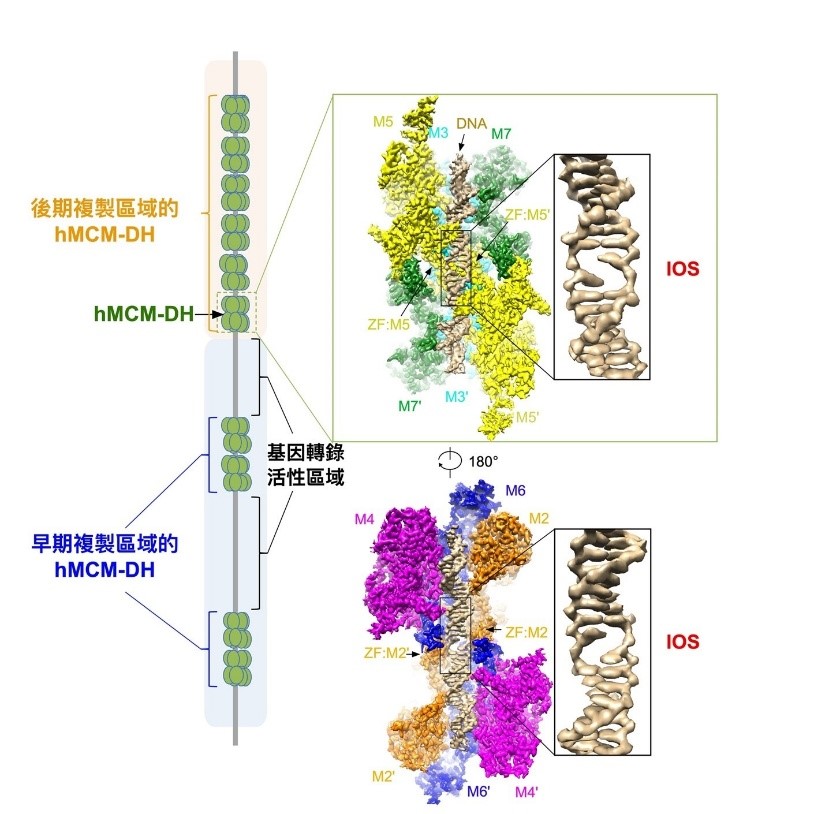
為了解開這個疑團,團隊使用當今最前沿的冷凍電鏡技術,研究以肉眼無法觀測的MCM2-7 DH原子分辨率的高分辨結構,從而了解該蛋白複合體的工作原理。在2015年,團隊首次解析了從釀酒酵母提純的MCM2-7 DH的冷凍電鏡結構,相關研究成果已在國際知名期刊《自然》上發表 (按此瀏覽期刊文章)。可惜的是,在該次研究中獲得的結構,其複製原點 DNA非常不穩定,因而無法提供其雙螺旋狀態的信息。幸而,該團隊近日終於成功純化出人源MCM2-7 DH複合物,並能解析其原子分辨率達2.59埃的高精度結構。該結構清晰地展示MCM2-7 DH聚合體直接降低DNA雙鏈的穩定性,並將位於兩個六聚體結合處的雙鏈DNA解旋,形成一個初始開口,從而將MCM2-7 DH牢固結合在初始打開的原點DNA上,遍佈整個基因組上沒有活躍的「信使RNA(mRNA)」轉錄的區域。該研究發現,如果DNA初始開口的結構被破壞或干擾,所有的 MCM2-7 DH將無法穩定地在DNA上結合,從而完全抑制DNA複製的起始。
「原子分辨率的冷凍電鏡結構使我們可以直接觀測到DNA的解離,這對於理解DNA複製的分子機制至關重要。」科大生命科學部助理教授黨尚宇博士說。「這項研究同時也說明了合作的重要性。為了解答最根本的生物學問題,往往需要來自具備不同專長的研究團隊共同努力。」
一直以來,DNA複製是多個癌症治療藥物的作用靶點。然而,由於現有藥物往往具有較大毒性,而正常細胞和癌症細胞均會在增殖過程中進行DNA複製,導致治療過程中,藥物無差別地殺死癌症細胞和正常細胞。
目前,如何提高化療藥物作用的針對性,一直是研發抗癌化合物的重要考量。在現階段,一個理想方案是通過抑制DNA複製起始,使正常細胞滯留在G1期(細胞分裂的一個階段)或者在G0期(細胞停止分裂的階段)靜止;在此情況下,癌症細胞則因其調控機制的紊亂,無法像正常細胞一樣被保護在相應的細胞週期,從而進入誘導細胞凋亡。因此,阻斷細胞複製起始,有望成為一種全新的、有效的、高度特異針對癌症細胞的抗癌療法。該研究揭示的人源複製前始複合物的蛋白結構和工作機制,為以MCM2-7複合體為靶點的無毒抗癌藥物開發提供了設計思路和重要的結構基礎。
研究團隊
研究團隊由港大生物科學學院的翟元樑博士領導,成員包括科大生命科學部的黨尚宇博士、科大高等研究院的戴楊碧瓘教授、法國居禮研究所的陳春龍博士、香港理工大學(理大)應用生物學和化學技術系的趙倩博士。
論文其他作者包括:港大生物科學學院的李健先生、范欣雨女士、許恩捷女士、李淑君博士、林瑋熙博士; 科大生命科學部的董江清博士、余大啟博士;法國居禮研究所的王緯韜博士、Nathan Alary先生;科大冷凍電鏡中心的張盈怡博士;理大應用生物學和化學技術系的楊陽先生。
鳴謝
這項研究中所有冷凍電鏡數據均在香港科技大學生物冷凍電鏡中心收集,該中心得到羅桂祥基金會的慷慨資助。兩位共同第一作者,董江清博士和余大啟博士獲得羅桂祥獎學金支持。
圖片下載及説明:https://www.scifac.hku.hk/press
傳媒查詢
香港大學理學院
杜之樺 ( 電話:3917-4948; 電郵:caseyto@hku.hk )
陳詩迪 ( 電話:3917-5286; 電郵:cindycst@hku.hk )
香港科技大學公共事務處
馮惠儀 ( 電話:2358-6307;電郵:fannyfung@ust.hk )