新闻及香港科大故事
2023
新闻
科大突破性发现罕见肿瘤细胞「间谍」 揭示不为人知的癌细胞
香港科技大学(科大)研究人员研发了一种可为冷冻和新鲜细胞组织样本同时进行单细胞DNA和RNA测序的新技术,更利用这方法识别出伪装为正常细胞的罕见脑肿瘤细胞「间谍」。是次发现为一些最复杂和罕见肿瘤的研究带来突破,并为未来的药物靶标发现开辟新方向。
肿瘤内的不同细胞基因和分子构造(即细胞异变质性)会影响癌症的病理以及肿瘤产生耐药性的能力,所以在决定癌症治疗方法前进行DNA 和 RNA 测序,可以取得有关肿瘤基因和分子组成的重要资讯。由于我们对癌症所知有限,透过分析DNA 和 RNA 测序所产生的更详细、不同层面的肿瘤分子数据,或可以对有关癌症的谜团,包括肿瘤复发或对治疗产生耐药性的原因提供更多的线索。目前,大部分现成的临床癌症样本是来自冷冻生物样本库的冷冻组织,这些样本目前可以用于肿瘤单细胞RNA测序分析,而利用现有技术对这些冷冻组织同时进行单细胞DNA 和 RNA 测序仍有一定的局限。
由科大生命科学学部及化学与生物工程学系副教授吴若昊教授及其博士后研究员于雷博士带领的团队开发了一种新型多功能单细胞多组学分析技术scONE-seq。这种技术不仅能分析冷冻细胞及难以取得的细胞类型,如骨胳和大脑;同时也大大简化了收集肿瘤中的DNA和RNA数据的实验流程。
星形胶质瘤(Astrocytoma)是一种致命且具扩散性的脑肿瘤,患有此类肿瘤的患者在确诊后五年内的存活率仅为 5% 左右。团队利用其新型单细胞技术,在星形胶质瘤患者样本中发现了一种细小而独特的肿瘤细胞亚群。这种独特的肿瘤细胞群体通过伪装成大脑的正常星形胶质细胞,逃过使用其他常见肿瘤测序方法的检测。此外,团队亦发现这种「间谍」肿瘤细胞具有耐药性分子特征;有关「间谍」肿瘤细胞在肿瘤恶化中所起的作用将是未来研究的重要方向。
新闻
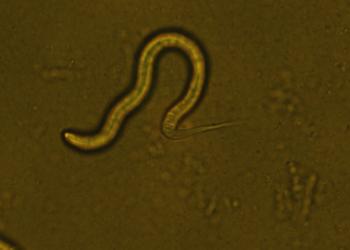
解构秀丽隐杆线虫pri-miRNA加工复合体的分子机制
小分子核糖核酸(microRNAs,以下简称miRNAs)是一种在动物和人类基因调控中发挥重要作用的小型核糖核酸(RNA),一直令许多科学家为之着迷。在生物学和医学中,一項非常重要的研究范畴就是miRNA如何控制和调节基因表达,因为科学界一般相信,这个课题对理解细胞突变有重大作用,对於治疗癌症和其他与细胞突变有关的疾病,至为关键。
虽然miRNA及其在人类中的生物起源已是科学界的热门题目,但针对其他动物中的miRNA加工复合体(一种启动miRNA生物起源的蛋白质复合物)的研究却相当缺乏。最近,香港科技大学(科大)的研究团队揭示了秀丽隐杆线虫加工复合体(cMP)的基本机制,该研究为未来线虫中miRNA相关研究铺平了道路,并为探索miRNA在所有生物中发挥的作用,提供更广泛的视觉。
该研究最近在开放获取期刊Nucleic Acids research上发表。
领导这项研究的科大生命科学部助理教授阮俊英教授说:「秀丽隐杆线虫加工复合体(cMP)的分子机制自18年前发现以来,一直没有详细阐明。当然,出于充分的理由,许多人关注于人源miRNA的研究,但是对于秀丽隐杆线虫中这种复合体卻缺乏基本信息,所以引发了我們的研究。」

新闻
隐藏深海的热浪对珊瑚礁构成威胁
2019年四月至五月,位于南太平洋中部法属坡利尼西亚莫雷阿岛一带的珊瑚礁经历了长时间且严重的高温白化。由于该年并非厄尔尼诺年份,一般并不会出现这种情况,因此本事件令全球海洋科学界百思不解。
由香港科技大学海洋科学系艾力克斯・怀亚特(Alex Wyatt)助理教授领衔的国际团队对这宗不寻常的珊瑚白化事件展开了调查。研究人员发现,这次灾难与反气旋涡流的通过有关。该涡流使该区域海平面升高,并使温度较高的海水集中在珊瑚礁上,进而导致海洋热浪大规模地隐藏在水面之下。团队的研究成果最近于《自然通讯》(Nature Communications)期刊上发表 。
过往关于珊瑚白化模式的研究,大多数仰赖于海水表面温度的测量。以这种方法收集数据,并未能全面了解海洋温度升高对海洋生态系统、乃至对热带珊瑚礁的威胁。虽然以卫星大范围的海表温度监测资料有其重要用途,却不能协助科学界监测海面数米以下区域的热能,亦无法探究在水表面之下,热能变化如何影响生态群聚。
新闻
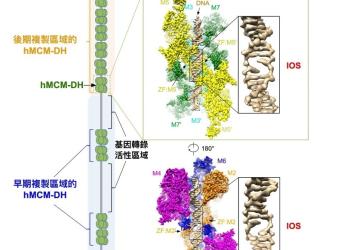
研究揭示DNA解旋机制 为癌症治疗带来新曙光
香港科技大学(科大)联同香港大学(港大)与法国居礼研究所共同发现了人体MCM2至MCM7蛋白复合体(Minichromosome Maintenance 2-7,微小染色体维持蛋白2-7)调控DNA 复制起始(Replication Initiation)的新机制。 此发现可被应用于研发新型、高效及更具针对性的抗癌药物。这项研究成果现已刊登在国际顶尖科学期刊《细胞》杂誌上(按此浏览期刊文章)。
我们的生命由单个受精卵细胞形成时开始。在母体子宫内,受精卵通过细胞分裂而发育成多细胞个体。在每次分裂中,编码遗传信息的基因组DNA都会被准确复制。每个细胞携带的DNA总长度约为两米,其通过摺叠、整合成为23对染色体。在人的一生中(约70年),人体将合成接近一光年长度的DNA(10^16米)。在复制的过程中,首先须利用解旋酶将双链DNA分解成两条单链DNA,其后DNA聚合酶以此为模板,合成两条新的互补配对的双螺旋DNA。若调控过程中出现一丝紊乱,都可能导致严重后果,例如肿瘤或遗传疾病等。
「破解DNA复制的机制是认识生命奥秘的关键。」领导这项研究的港大生物科学学院助理教授翟元樑博士说。「而解析复制机器蛋白质结构是了解其分子功能最核心的步骤,因为只有亲眼看到,才能相信。」
2022
新闻
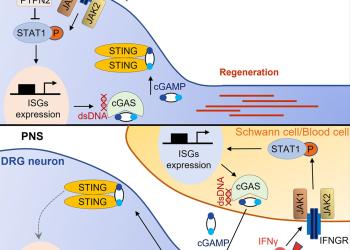
研究发现促进成年神经系统轴突再生的内在免疫机制
中枢神经系统一旦受创,例如在脊髓损伤的意外中,伤者很可能会永久丧失感觉或活动能力,当中的关键原因,是轴突断裂后无法再生。目前,医学界为脊髓损伤患者恢復活动能力的方法非常有限。若要为他们带来治疗希望,其中一个研究方向,便是要破解令这些受伤轴突再生的方法。
由香港科技大学(科大)生命科学部郑氏理学副教授刘凯带领的团队,用老鼠进行实验,解构了促进神经突轴再生的部分原理。他们发现,通过敲除神经元内编码一种磷酸酶的基因PTPN2,可以促进中枢神经系统的轴突重生,另外,若再外加Ⅱ型干扰素IFNγ,更可进一步提升再生的轴突数量和生长速度。这项研究的结果,最近于科学期刊Neuron上发表。
人类的神经系统可分为两部分:中枢神经系统和外周神经系统。与中枢神经系统的分别是,外周神经当受到损伤时,具有较强的再生和自我修復能力 。不过,科学界一直并未完全了解这个再生和修復过程与神经系统内在免疫机制以及免疫相关的细胞因子的关係,包括一些信号通路如何影响受伤的神经元,以及它们能否直接促进轴突再生。
是项研究亦探索了IFNγ-cGAS-STING信号通路有否参与外周神经的自我修復过程。团队发现,外周神经轴突可以在损伤后,直接调节其损伤环境中的免疫反应,以促进自我修復。
在过往的研究中,刘教授的团队已经发现,可以通过提高神经元电活动,改变神经元甘油脂代谢途径等不同方法,从而加强轴突的再生能力。今次这项研究,为脊髓损伤这类情况的未来治疗方案,找到进一步线索,比如联合几种不同的信号通路可以大幅提高神经再生。

新闻
科大团队开发一种新型集成方案实现 III-V半导体器件和硅组件之间的有效耦合
香港科技大学的研究人员最近发明了一种新型集成方案,透过选择性直接外延技术1,在硅光子平台上开发了III-V族化合物半导体器件和硅组件的高效耦合—,释放集成高能效光子和低成本电子的潜能,令下一代通信 可以低成本、更高速和更大容量的方式呈现。
近年,在大数据、汽车、云端和传感器等各种应用和新兴技术的推动下,数据流量呈指数级增长。为了解决数据通信的瓶颈,硅光子学成为一项被广泛研究的核心技术,通过节能、大容量和低成本的光互连实现数据传输的增长。虽然硅基无源组件已经在硅光子平台上成熟的建立,但激光器和光电探测器并不能由硅制成,需要在硅上集成其他材料,例如 III-V 族化合物半导体等。
现时对于硅上的 III-V 激光器和光电探测器主要通过两种方法进行了研究。第一个是以键合为基础的方法,尽管此方法已能产出了性能很好的器件,但要求复杂的制造工艺,而且成本高、产量低,使大规模生产变得非常具挑战性。另一种方法是通过在硅上纵向生长多层 III-V 的直接外延方法,虽然它提供了一种成本更低、可扩展性更大和集成密度更高的解决方案,然而这种方法中所必须用到的几微米厚的 III-V 缓冲层阻碍了 III-V 和硅之间的有效光耦合,因此解决这一问题成为了集成硅光子学的关键。
为解决这一关键问题,由香港科技大学电子及计算器工程学系荣休教授刘纪美领导的团队开发了横向选区生长技术—一种新颖的选择性直接外延方法,可以选择性地在硅上横向生长 III-V 材料,而无需缓冲层。此外,基于这项新技术,该团队亦设计并实现了 III-V 光电探测器和硅组件的独特面内集成,并在 III-V 和硅之间具有高耦合效率。与商用光电探测器相比,这种方法实现的光电探测器噪声更小,灵敏度更高,工作范围更广,且具有超过 112 Gb/s的高速—较现有产品更快。这不但乃首次通过直接外延的方法实现III-V 器件与硅组件的有效耦合,而且可以应用于各种 III-V 器件和硅基组件的集成,从而实现在硅光子平台上集成光与电模块以进行数据通信的最终目标。

新闻
科大团队破解干细胞变化之谜 为抗衰老研究迈进一大步
古今中外,「抗衰老」一直都是历史和文学中的热门题材。从中国古代的秦始皇派员远征大海寻找长生不死之药,到西方小说中的德古拉伯爵拥有不死之身,千百年来,人类仍沉醉于寻找不老之术,至今仍未有解决方法。
最近,由何善衡生命科学教授席生命科学部副教授张晓东教授领导的一个研究小组,在抗衰老研究上获得了突破性的进展。
张教授一直专注于研究肌肉干细胞。肌肉干细胞在人体的肌肉修复过程中,起着关键的作用,而团队发现了一种方法,可基于染色质的特征识别出老化的肌肉干细胞。衰老的肌肉干细胞与年轻的不同,它们的干性会降低,也就是说它们成为新干细胞或变成特定细胞以替代受损组织的能力会降低。在下一步的研究中,如果能再找到方法将这些衰老细胞的染色质特征修改,将它们变得与年轻细胞一样的话,那么细胞衰老、以致骨胳肌组织衰老的过程便有望暂停,甚至逆转。
团队的研究成果最近于Cell Press 出版的公开期刊 iScience 中发表。
张教授认为,调控染色质的开放程度及可及性是决定细胞命运的关键。他阐释说,染色质状态的变化可导致基因表达失调。今次的研究显示逐渐激活的染色质状态是干细胞衰老的重要标志,而这项发现很可能成为未来研发抗衰老技术的一个重要方向。
染色质是一种包裹在组蛋白周围的 DNA 复合物,用于维持 DNA 的正常结构,而它们的结构会随外部环境迅速变化。承接以往研究所得,团队今次在老鼠体内预先固定了肌肉干细胞的状态,以取得静息细胞(平时在休眠状态, 但在肌肉受伤时会激活,以发挥修复功能)以及它们的基因和染色质特征,再随着时间变化,比较染色质的「可及性」。
研究的第一作者董安琪博士指出:「我们发现年轻肌肉干细胞的染色质环境,在静息状态会变得非常紧密,并在激活初期有较高的『可及性』。它们在长期的再生过程后,会逐渐重新建立紧密状态。然而,老化的肌肉干细胞在静息期间,则不能维持染色质的紧密环境。」董博士是张教授研究团队的前成员,现为布鲁塞尔自由大学博士后研究员。







